在医药、医疗器械及食品等对无菌要求极高的行业,灭菌工艺及其设备的验证是确保产品安全、有效、合规的核心环节。传统的验证过程依赖大量线下操作、纸质记录和人工监控,不仅耗时耗力,还存在数据追溯难、效率低下等问题。随着工业互联网与数字技术的发展,网络技术服务正为灭菌工艺及设备验证带来深刻的变革,构建起更智能、高效、可靠的质量保障体系。
一、 灭菌工艺验证:从线下到云端的精准管控
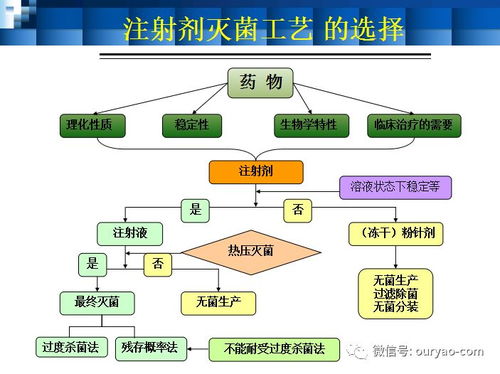
灭菌工艺验证旨在证明所采用的灭菌方法(如湿热灭菌、干热灭菌、辐射灭菌、环氧乙烷灭菌等)能够持续、稳定地达到预定的无菌保证水平(SAL)。网络技术服务的介入,主要体现在:
- 验证方案与数据的数字化管理:通过部署在云端的验证管理平台,企业可以标准化验证方案(如安装确认IQ、运行确认OQ、性能确认PQ)的模板、审批流程和执行路径。验证过程中产生的温度、压力、时间、生物指示剂培养结果等海量数据,可经由物联网(IoT)传感器自动采集并实时上传至平台,杜绝人工抄录错误,确保数据完整性与真实性(符合ALCOA+原则)。
- 过程模拟与智能分析:利用云计算能力,可以对灭菌腔室内的温度分布、热穿透情况进行高级数据分析和可视化呈现。通过历史数据训练模型,网络平台能对验证结果进行智能判读,预警潜在的风险点(如冷点区域),甚至模拟不同装载方式下的灭菌效果,为优化工艺参数提供数据驱动的决策支持。
- 远程协作与审计支持:验证工作往往需要设备供应商、第三方检测机构及企业内部多部门协作。网络协作工具与平台支持远程监控验证过程、实时共享数据与报告,极大提升了协作效率。所有电子记录均带有时间戳和防篡改功能,为应对国内外药监机构(如FDA、NMPA)的远程审计或现场审计提供了完整、清晰、可即时检索的证据链。
二、 灭菌设备验证:全生命周期的联网运维
灭菌设备本身的性能确认与持续维护是工艺稳定的基础。网络技术服务将其升级为“智能设备”的全生命周期管理:
- 安装与运行确认的智能化:新设备安装后,其关键仪表校准数据、设备运行参数等可直接联网录入系统,与预设的标准进行自动比对,快速完成IQ/OQ。设备自带的智能诊断系统可通过网络将状态信息反馈给制造商和用户,实现预测性维护。
- 性能确认的持续监控与再验证:传统PQ通常定期进行(如每年一次)。而通过网络连接,设备的关键运行参数(如灭菌阶段的温度曲线、真空泄漏率)可以被持续监控。系统可设定警戒限和行动限,一旦数据趋势出现异常偏差,即刻自动报警并触发调查或预防性维护流程,将“定期再验证”部分转化为“持续验证”,更主动地保障设备始终处于验证过的状态。
- 设备集群与知识库联网:对于拥有多台、多地灭菌设备的企业,网络平台可以实现对所有设备的集中仪表盘管理,对比分析不同设备的性能效率。平台能够积累形成“灭菌验证知识库”,将成功的验证案例、故障处理经验、法规更新要求等数字化沉淀,为后续的验证活动和新厂建设提供宝贵的参考。
三、 网络技术服务的实施架构与安全考量
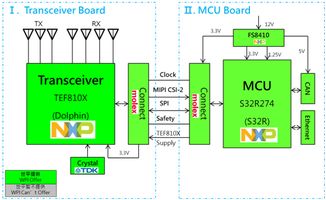
构建服务于灭菌验证的网络体系,通常采用分层架构:
- 感知层:由部署在灭菌器、生物指示剂培养箱、环境监测点的高精度智能传感器构成,负责数据采集。
- 网络层:通过工业网关、5G或有线网络将数据安全传输至平台。
- 平台层:核心是部署于私有云或合规公有云的验证管理软件平台,负责数据存储、处理、分析与可视化。
- 应用层:为验证工程师、质量负责人、审计官等不同角色提供Web端或移动端的交互界面。
安全与合规是生命线。系统必须满足《药品生产质量管理规范》(GMP)、数据完整性要求以及网络安全等级保护制度。措施包括但不限于:网络隔离、数据加密传输与存储、严格的权限管理与访问审计、异地备份以及符合GxP要求的电子签名功能。
结论
网络技术服务正将灭菌工艺及设备验证从一项孤立的、周期性的合规任务,转变为一个集成的、连续的、数据驱动的质量管理过程。它通过数字化、自动化与智能化,显著提升了验证工作的效率、可靠性与合规水平,降低了人为差错与质量风险。对于制药和医疗器械企业而言,积极拥抱和部署这些网络技术服务,不仅是提升自身质量体系成熟度的关键步骤,也是在日益严格的全球监管环境下构建核心竞争力的战略选择。随着人工智能与工业元宇宙技术的进一步发展,灭菌验证有望实现更高程度的虚拟仿真与自主优化,持续为产品安全保驾护航。